ELEMENTOS DE LA TABLA PERIÓDICA 4-5-6-7 PERIODO 2
INTRODUCCIÓN
En este trabajo se podrán observar 24 elementos de la tabla periódica,en los cuales cada párrafo se responderán preguntas sobre que es,cuales son sus usos y características entre otras informaciones.
OBJETIVOS
- Identificar alguna característica en especial sobre los elementos
- Descubrir sus usos
- Reconocer que elemento es perjudicial para el medio ambiente
MARCO TEÓRICO
Carbono,Nitrógeno,Oxigeno,Flúor
Son los elementos químicos presentes en la segunda fila (o periodo) de la tabla periódica. La tabla periódica está compuesta de filas en función de tendencias recurrentes (periódicas) en el comportamiento químico de los elementos a medida que aumenta el número atómico: se comienza una hilera nueva cuando el comportamiento químico vuelve a repetirse, lo que significa que los elementos de comportamiento similar se encuentran en las mismas columnas verticales. El segundo período contiene más elementos que la hilera anterior, con ocho elementos: Litio, Berilio, Boro, Carbono, Nitrógeno, Oxígeno, Flúor y Neón.
CARBONO


El carbono (C) es un elemento químico de número atómico 6. Es sólido a temperatura ambiente. Dependiendo de las condiciones de formación, puede encontrarse en la naturaleza en distintas formas alotrópicas, carbono amorfo y cristalino en forma de grafito o diamante. Es el pilar básico de la química orgánica; se conocen cerca de 15 millones de compuestos de carbono, aumentando este número en unos 500.000 compuestos por año, y forma parte de todos los seres vivos conocidos. Forma el 0,2 % de la corteza terrestre. El carbono es un elemento notable por varias razones. Sus formas alotrópicas incluyen, sorprendentemente, una de las sustancias más blandas (el grafito) y la más dura (el diamante) y, desde el punto de vista económico, uno de los materiales más baratos (carbón) y uno de los más caros (diamante). Más aún, presenta una gran afinidad para enlazarse químicamente con otros átomos pequeños, incluyendo otros átomos de carbono con los que puede formar largas cadenas, y su pequeño radio atómico le permite formar enlaces múltiples. Así, con el oxígeno forma el óxido de carbono (IV), vital para el crecimiento de las plantas (ver ciclo del carbono); con el hidrógeno forma numerosos compuestos denominados genéricamente hidrocarburos, esenciales para la industria y el transporte en la forma de combustibles fósiles; y combinado con oxígeno e hidrógeno forma gran variedad de compuestos como, por ejemplo, los ácidos grasos, esenciales para la vida, y los ésteres que dan sabor a las frutas; además es vector, a través del ciclo carbono-nitrógeno, de parte de la energía producida por el sol.
Características
- El carbono es un elemento notable por varias razones. Sus formas alotrópicas incluyen, una de las sustancias más blandas (el grafito) y una de las más duras (el diamante) y, desde el punto de vista económico, es de los materiales más baratos (carbón) y uno de los más caros (diamante). Más aún, presenta una gran afinidad para enlazarse químicamente con otros átomos pequeños, incluyendo otros átomos de carbono con los que puede formar largas cadenas, y su pequeño radio atómico le permite formar enlaces múltiples. Así, con el oxígeno forma el dióxido de carbono, vital para el crecimiento de las plantas (ver ciclo del carbono); con el hidrógeno forma numerosos compuestos denominados genéricamente hidrocarburos, esenciales para la industria y el transporte en la forma de combustibles fósiles; y combinado con oxígeno e hidrógeno forma gran variedad de compuestos como, por ejemplo, los ácidos grasos, esenciales para la vida, y los ésteres que dan sabor a las frutas; además es vector, a través del ciclo carbono-nitrógeno, de parte de la energía producida por el sol
Estados alotrópicos
Una de las formas en las cuales se encuentra el carbono es el grafito, caracterizado por tener sus átomos "en los vértices de hexágonos que tapizan un plano",es de color negro, opaco y blando, y es el material del cual está hecha la parte interior de los lápices de madera. El grafito tiene exactamente los mismos átomos del diamante, pero por estar dispuestos en diferente forma tienen distintas propiedades físicas y químicas. Los diamantes naturales se forman en lugares donde el carbono ha sido sometido a grandes presiones y altas temperaturas. Su estructura es tetraédrica, que da como resultado una red tridimensional y a diferencia del grafito tiene un grado de dureza alto: 10 Mohs. Los diamantes se pueden crear artificialmente, sometiendo el grafito a temperaturas y presiones muy altas. El precio del grafito es menor al de los diamantes naturales, pero si se han elaborado adecuadamente tienen la misma dureza, color y transparencia.La forma amorfa es esencialmente grafito, pero no llega a adoptar una estructura cristalina macroscópica. Esta es la forma presente en la mayoría de los carbones y en el hollín.A presión normal, el carbono adopta la forma del grafito, en la que cada átomo está unido a otros tres en un plano compuesto de celdas hexagonales; este estado se puede describir como 3 electrones de valencia en orbitales híbridos planos sp² y el cuarto en el orbital p.
Las dos formas de grafito conocidas alfa (hexagonal) y beta (romboédrica) tienen propiedades físicas idénticas. Los grafitos naturales contienen más del 30 % de la forma beta, mientras que el grafito sintético contiene únicamente la forma alfa. La forma alfa puede transformarse en beta mediante procedimientos mecánicos, y esta recristalizar en forma alfa al calentarse por encima de 1000 °C.Debido a la deslocalización de los electrones del orbital pi, el grafito es conductor de la electricidad, propiedad que permite su uso en procesos de electroerosión. El material es blando y las diferentes capas, a menudo separadas por átomos intercalados, se encuentran unidas por enlaces de Van de Waals, siendo relativamente fácil que unas deslicen respecto de otras, lo que le da utilidad como lubricante.
A muy altas presiones, el carbono adopta la forma del diamante, en el cual cada átomo está unido a otros cuatro átomos de carbono, encontrándose los 4 electrones en orbitales sp³, como en los hidrocarburos. El diamante presenta la misma estructura cúbica que el silicio y el germanio y, gracias a la resistencia del enlace químico carbono-carbono, es, junto con el nitruro de boro, la sustancia más dura conocida. La transición a grafito a temperatura ambiente es tan lenta que es indetectable. Bajo ciertas condiciones, el carbono cristaliza como lonsdaleíta, una forma similar al diamante pero hexagonal.
El orbital híbrido sp1 que forma enlaces covalentes solo es de interés en química, manifestándose en algunos compuestos, como por ejemplo el acetileno.
Fullereno C60.
Los fullerenos fueron descubiertos hace 15 años tienen una estructura similar al grafito, pero el empaquetamiento hexagonal se combina con pentágonos (y en ciertos casos, heptágonos), lo que curva los planos y permite la aparición de estructuras de forma esférica, elipsoidal o cilíndrica. El constituido por 60 átomos de carbono, que presenta una estructura tridimensional y geometría similar a un balón de fútbol, es especialmente estable. Los fullerenos en general, y los derivados del C60 en particular, son objeto de intensa investigación en química desde su descubrimiento a mediados de los 1980.
Aplicaciones
El principal uso industrial del carbono es como un componente de hidrocarburos, especialmente los combustibles fósiles (petróleo y gas natural). Del primero se obtienen, por destilación en las refinerías, gasolinas, queroseno y aceites, siendo además la materia prima empleada en la obtención de plásticos. El segundo se está imponiendo como fuente de energía por su combustión más limpia.
- El grafito se combina con arcilla para fabricar las minas de los lápices. Además se utiliza como aditivo en lubricantes. Las pinturas anti-radar utilizadas en el camuflaje de vehículos y aviones militares están basadas igualmente en el grafito, intercalando otros compuestos químicos entre sus capas. Es negro y blando. Sus átomos están distribuidos en capas paralelas muy separadas entre sí. Se forma a menos presión que el diamante. Aunque parezca difícil de creer, un diamante y la mina de un lapicero tienen la misma composición química: carbono.
- El diamante es transparente y muy duro. En su formación, cada átomo de carbono está unido de forma compacta a otros cuatro átomos. Se originan con temperaturas y presiones altas en el interior de la tierra. Se emplea para la construcción de joyas y como material de corte aprovechando su dureza.
- Como elemento de aleación principal de los aceros.
- Las pastillas de carbón se emplean en medicina para absorber las toxinas del sistema digestivo y como remedio de la flatulencia.
- El carbón activado se emplea en sistemas de filtrado y purificación de agua.
SILICIO


Elemento químico metaloide, número atómico 14 y situado en el grupo 4 de la tabla periódica de los elementos formando parte de la familia de los carbonoideos de símbolo Si. Es el segundo elemento más abundante en la corteza terrestre (27,7% en peso) después del oxígeno. Se presenta en forma amorfa y cristalizada; el primero es un polvo parduzco, más activo que la variante cristalina, que se presenta en octaedros de color azul grisáceo y brillo metálico.
Características principales
- Sus propiedades son intermedias entre las del carbono y el germanio. En forma cristalina es un muy duro y poco soluble y presenta un brillo metálico y color grisáceo. Aunque es un elemento relativamente inerte y resiste la acción de la mayoría de los ácidos, reacciona con los halógenos y álcalis diluidos. El silicio transmite más del 95% de las longitudes de onda de la radiación infrarroja.
- Se prepara en forma de polvo amarillo pardo o de cristales negros-grisáceos. Se obtiene calentando sílice, o dióxido de silicio (SiO2), con un agente reductor, como carbono o magnesio, en un horno eléctrico.El silicio cristalino tiene una dureza de 7, suficiente para rayar el vidrio, de dureza de 5 a 7. El silicio tiene un punto de fusión de 1.411 °C, un punto de ebullición de 2.355 °C y una densidad relativa de 2,33(g/ml). Su masa atómica es 28,086 u (unidad de masa atómica).
- Se disuelve en ácido fluorhídrico formando el gas tetrafluoruro de silicio, SiF4 (ver flúor), y es atacado por los ácidos nítrico, clorhídrico y sulfúrico, aunque el dióxido de silicio formado inhibe la reacción. También se disuelve en hidróxido de sodio, formando silicato de sodio y gas hidrógeno. A temperaturas ordinarias el silicio no es atacado por el aire, pero a temperaturas elevadas reacciona con el oxígeno formando una capa de sílice que impide que continúe la reacción. A altas temperaturas reacciona también con nitrógeno y cloro formando nitruro de silicio y cloruro de silicio, respectivamente.
- Se disuelve en ácido fluorhídrico formando el gas tetrafluoruro de silicio, SiF4 (ver flúor), y es atacado por los ácidos nítrico, clorhídrico y sulfúrico, aunque el dióxido de silicio formado inhibe la reacción. También se disuelve en hidróxido de sodio, formando silicato de sodio y gas hidrógeno. A temperaturas ordinarias el silicio no es atacado por el aire, pero a temperaturas elevadas reacciona con el oxígeno formando una capa de sílice que impide que continúe la reacción. A altas temperaturas reacciona también con nitrógeno y cloro formando nitruro de silicio y cloruro de silicio, respectivamente.
- El silicio constituye un 28 % de la corteza terrestre. No existe en estado libre, sino que se encuentra en forma de dióxido de silicio y de silicatos complejos. Los minerales que contienen silicio constituyen cerca del 40 % de todos los minerales comunes, incluyendo más del 90 % de los minerales que forman rocas volcánicas. El mineral cuarzo, sus variedades (cornalina, crisoprasa, ónice, pedernal y jaspe) y los minerales cristobalita y tridimita son las formas cristalinas del silicio existentes en la naturaleza. El dióxido de silicio es el componente principal de la arena. Los silicatos (en concreto los de aluminio, calcio y magnesio) son los componentes principales de las arcillas, el suelo y las rocas, en forma de feldespatos, anfíboles, piroxenos, micas y zeolitas, y de piedras semipreciosas como el olivino, granate, zircón, topacio y turmalina.
Aplicaciones
Se utiliza en aleaciones, en la preparación de las siliconas, en la industria cerámica y debido a que es un material semiconductor muy abundante, tiene un interés especial en la industria electrónica y microelectrónica como material básico para la creación de obleas o chips en los que se pueden implementar transistores, pilas solares, y una gran variedad de circuitos electrónicos.
GERMANIO


El germanio (antiguamente llamado eka-silicio) es un elemento químico con número atómico 32, y símbolo Ge perteneciente al período 4 de la tabla periódica de los elementos.
Características principales
Es un semimetal, de color blanco grisáceo lustroso, quebradizo, que conserva el brillo a temperaturas ordinarias. Presenta la misma estructura cristalina que el diamante y resiste a los ácidos y álcalis.
Forma gran número de compuestos organometálicos y es un importante material semiconductor utilizado en transistores y fotodetectores. A diferencia de la mayoría de semiconductores, el germanio tiene una pequeña banda prohibida (band gap) por lo que responde de forma eficaz a la radiación infrarroja y puede usarse en amplificadores de baja intensidad.
Aplicaciones
- Fibra óptica
- Óptica de infrarrojos: Espectroscopios, sistemas de visión nocturna y otros equipos.
- En joyería se usa la aleación Au con 12% de germanio.
- Como elemento endurecedor del aluminio, magnesio y estaño.
ESTAÑO
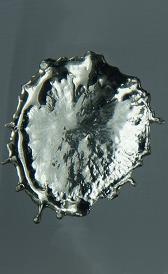

El estaño es un elemento químico de símbolo Sn (del latín stannum) y número atómico 50. Está situado en el grupo 14 de la tabla periódica de los elementos. Se conocen 10 isótopos estables. Su principal mena es la casiterita.
Características
- Es un metal blanco, maleable, que se oxida fácilmente, a temperatura ambiente, cambiando de color a un gris más opaco, y es resistente a la corrosión. Se encuentra en muchas aleaciones y se usa para recubrir otros metales protegiéndolos de la corrosión. Al doblar una barra de este metal se produce un sonido característico llamado grito del estaño, producido por la fricción de los cristales que la componen. Una de sus características más llamativas es que bajo determinadas condiciones sufre la peste del estaño. Por debajo de los -18°C empieza a descomponerse y a convertirse en un polvo gris; a este proceso se lo conoce como peste del estaño. El estaño puro tiene dos variantes alotrópicas: el estaño gris, polvo no metálico, semiconductor, de estructura cúbica y estable a temperaturas inferiores a 13,2 °C, que es muy frágil y tiene un peso específico más bajo que el blanco. El estaño blanco, el normal, metálico, conductor eléctrico, de estructura tetragonal y estable a temperaturas por encima de 13,2 °C.
Usos
- Se usa como protector del oro, del acero y de diversos metales usados en la fabricación de latas de conserva.
- También se usa para disminuir la fragilidad del vidrio.
- Los compuestos de estaño se usan para fungicidas, tintes, dentífricos y pigmentos.
- Se usa para realizar bronce, aleación de estaño y cobre.
- Se usa para la soldadura blanda, aleado con plomo.
- Se usa en aleación con plomo para fabricar la lámina de los tubos de los órganos musicales.
- Tiene utilidad en etiquetas.
- Recubrimiento de acero.
- Se usa como material de aporte en soldadura blanda con cautín, bien puro o aleado. La directiva RoHS prohíbe el uso de plomo en la soldadura de determinados aparatos eléctricos y electrónicos.
- El estaño también se utiliza en la industria de la cerámica para la fabricación de los esmaltes cerámicos. Su función es la siguiente: en baja y en alta es un opacificante. En alta la proporción del porcentaje es más alto que en baja temperatura.
- Es usado también en el sobretaponado de botellas de vino, en forma de cápsula. Su uso se extendió tras la prohibición del uso del plomo en la industria alimentaria. España es uno de los mayores fabricantes de cápsulas de estaño.
Efectos toxicologicos
Tanto el estaño metálico como sus compuestos orgánicos e inorgánicos, ya sean formados de manera natural o en sus usos industriales, puede producir efectos tóxicos sobre el medio ambiente y los seres vivos expuestos a ellos.
El estaño es liberado en el medio ambiente por procesos naturales y por las actividades humanas, tales como la minería, la combustión de petróleo y carbón, además de las actividades industriales asociadas a la producción y usos del estaño.
El estaño metálico cuando se encuentra en la atmósfera en forma gaseosa se adhiere a las partículas de polvo, las cuales pueden ser movilizadas por la acción del viento la lluvia o la nieve.
Cuando se libera el estaño metálico en el medio ambiente, este se puede unir con el cloro, azufre u oxígeno para formar compuestos inorgánicos de estaño, tales como el cloruro de estaño, sulfuro de estaño, u dióxido de estaño. Este tipo de compuestos no pueden ser degradados y solo pueden cambiar su forma química, de manera que son adheridos por el suelo y los sedimentos o son disueltos en el agua.
Cuando se combina con el carbono puede formar compuestos orgánicos tales como dibutilestaño, tributilo de estaño y el trifenilestaño. Este tipo de compuestos pueden ser acumulados en el suelo o en el agua, o ser degradados a compuestos inorgánicos por la acción de la luz solar o las bacterias. El tiempo de permanencia en el medio de estos compuestos es variable en función del compuesto, pudiendo ser desde días hasta meses en el agua, y años si se encuentran en el suelo. Debido a su forma química los compuestos orgánicos de estaño también pueden bioacumularse al ser asimilado por el metabolismo de los seres vivos, sufriendo un proceso de biomagnificación a lo largo de las diferentes redes tróficas.
PLOMO


El plomo es un elemento químico de la tabla periódica, cuyo símbolo es Pb (del latín plumbum) y su número atómico es 82 según la tabla actual, ya que no formaba parte en la tabla periódica de Mendeleiev. Este químico no lo reconocía como un elemento metálico común por su gran elasticidad molecular. Cabe destacar que la elasticidad de este elemento depende de la temperatura ambiente, la cual extiende sus átomos.
El plomo es un metal pesado de densidad relativa o gravedad específica 11,4 a 16 °C, de color plateado con tono azulado, que se empaña para adquirir un color gris mate. Es flexible, inelástico y se funde con facilidad. Su fusión se produce a 327,4 °C y hierve a 1725 °C. Las valencias químicas normales son 2 y 4. Es relativamente resistente al ataque del ácido sulfúrico y del ácido clorhídrico, aunque se disuelve con lentitud en ácido nítrico y ante la presencia de bases nitrogenadas. El plomo es anfótero, ya que forma sales de plomo de los ácidos, así como sales metálicas del ácido plúmbico. Tiene la capacidad de formar muchas sales, óxidos y compuestos organometálicos.
Características generales
- Los compuestos de plomo más utilizados en la industria son los óxidos de plomo, el tetraetilo de plomo y los silicatos de plomo. El plomo forma aleaciones con muchos metales, y, en general, se emplea en esta forma en la mayor parte de sus aplicaciones. Es un metal pesado y tóxico, y la intoxicación por plomo se denomina como saturnismo o plumbosis.
- El plomo en la naturaleza nunca se halla en su estado puro, sino formando sales metálicas, óxidos y compuestos organometálicos.
- La mayoría de los minerales de los que se extrae contienen un porcentaje entre 3 y 10% de plomo.
Toxicidad
El plomo es un material tóxico, capaz de contaminar el cuerpo y provocar una enfermedad conocida como plumbosis o saturnismo. El plomo se absorbe por vía cutánea, respiratoria y digestiva, afectando los sistemas nervioso y renal.
Para el organismo, eliminar esta sustancia resulta difícil y costoso. Por eso, ante elevados niveles de absorción el pronóstico es bastante sombrío.
Entre sus posibles efectos adversos figuran el daño renal, la anemia por destrucción de la hemoglobina sanguínea, daño cerebral, vértigos, vómitos, diarreas, abortos, disminución de la fertilidad y dificultades de aprendizaje en niños.
Su efecto en el sistema nervioso puede observarse también en alteraciones en el comportamiento. Por ejemplo, puede provocar agresividad, hipersensibilidad o comportamiento impulsivo.
Riesgo ambiental
El plomo es un potente contaminante que se ha detectado incluso entre las aguas congeladas de los polos terrestres. Su elevada concentración ambiental se debe a las actividades industriales humanas, en especial a su adición al proceso de combustión de motores. Por eso, se lo ha prohibido como aditivo en la gasolina.
El envenenamiento de los animales con plomo les restringe sus capacidades innatas de geolocalización, de equilibrio y magnetocepción. Además, induce a mutaciones, así como comportamientos erráticos y agresivos.
UNUNQUADIO

Fue producido por primera vez por los científicos que trabajan en el Instituto Joint de Investigación Nuclear en Dubnia, Rusia, en 1998. Bombardearon átomos de plutonio con iones de calcio. Esto produjo un único átomo de Ununquadio 289, un isótopo con una vida media de alrededor de 21 segundos.
Hasta la fecha se han observado alrededor de 80 desintegraciones de átomos de flerovio, 50 de ellas directamente y 30 de la desintegración de los elementos más pesados Livermorio y Oganesón. Todas las desintegraciones han sido asignados a los cuatro isótopos vecinos con números de masa 286-289. El isótopo de más larga vida conocido actualmente es el 289Fl114 con una vida media de aproximadamente 2,6 s, aunque hay evidencias de un isómero, 289bFl114, con una vida media de aproximadamente 66 s, que sería uno de los núcleos más longevos en la región de los elementos superpesados.
Experimentos químicos muy recientes han indicado fuertemente que el elemento 114 no posee propiedades 'eka'-plomo y parece comportarse como el primer elemento superpesado, que presenta propiedades similares a los gases nobles debido a efectos relativistas.
Isotopo
El isótopo más estable del ununquadio, el Ununquadio 289, tiene una vida media de unos 21 segundos. Se desintegra en ununbio 285 emitiendo partículas alfa.
Ya que solo unos pocos átomos de Ununquadio han sido producidos, actualmente no tiene ningún uso a parte de los relativos a investigación científica.
NITRÓGENO


El nitrógeno es un elemento químico de número atómico 7, símbolo N, su peso atómico es de 14,006 y que en condiciones normales forma un gas diatómico (nitrógeno diatómico o molecular) que constituye del orden del 78 % del aire atmosférico.En ocasiones es llamado ázoe (antiguamente se usó también Az como símbolo del nitrógeno).
El nitrógeno tiene una elevada electronegatividad (3,04 en la escala de Pauling) y, cuando tiene carga neutra, 5 electrones en el nivel más externo, comportándose como trivalente en la mayoría de los compuestos estables que forma. Existen dos isótopos estables del nitrógeno, N-14 y N-15,25 siendo el primero —que se produce en el ciclo carbono-nitrógeno de las estrellas— el más común sin lugar a dudas (99,634%).25 De los diez isótopos que se han sintetizado, uno tiene un periodo de semidesintegración de nueve minutos (el N-13), y el resto de segundos o menos. Con el hidrógeno forma el amoníaco (NH3),la hidracina (N2H4) y el aziduro de hidrógeno (N3H, también conocido como azida de hidrógeno o ácido hidrazoico). El amoníaco líquido, anfótero como el agua, actúa como una base en una disolución acuosa,formando iones amonio (NH4), y se comporta como un ácido en ausencia de agua, cediendo un protón a una base y dando lugar al anión amida (NH2). También se conocen largas cadenas y compuestos cíclicos de nitrógeno, pero son muy inestables. Con los halógenos forma: NF3, NF2Cl, NFCl2, NCl3, NBr3.6 NH3, NI3.6 NH3, N2F4, N2F2 (cis y trans), N3F, N3Cl, N3Br y N3I.
El nitrógeno es el componente principal de la atmósfera terrestre (78,1% en volumen) y se obtiene para usos industriales de la destilación del aire líquido. Está presente también en los restos de animales, por ejemplo el guano, usualmente en la forma de urea, ácido úrico y compuestos de ambos.Éste ocupa el 3% de la composición elemental del cuerpo humano. Se han observado compuestos que contienen nitrógeno en el espacio exterior y el isótopo Nitrógeno-14 se crea en los procesos de fusión nuclear de las estrellas. El nitrógeno es componente esencial de los aminoácidos y los ácidos nucleicos, vitales para la vida y los seres vivos.Las legumbres son capaces de absorber el nitrógeno directamente del aire, siendo éste transformado en amoníaco y luego en nitrato por bacterias que viven en simbiosis con la planta en sus raíces. El nitrato es posteriormente utilizado por la planta para formar el grupo amino de los aminoácidos de las proteínas que finalmente se incorporan a la cadena trófica (véase también el ciclo del nitrógeno).
La aplicación comercial más importante del nitrógeno diatómico es la obtención de amoníaco por el proceso de Haber.El amoníaco se emplea con posterioridad en la fabricación de fertilizantes y ácido nítrico. Las sales del ácido nítrico incluyen importantes compuestos como el nitrato de potasio (nitro o salitre empleado en la fabricación de pólvora) y el nitrato de amonio fertilizante. Los compuestos orgánicos de nitrógeno como la nitroglicerina y el trinitrotolueno son a menudo explosivos.La hidracina y sus derivados se usan como combustible en cohetes.
El ciclo de este elemento es bastante más complejo que el del carbono, dado que está presente en la atmósfera no sólo como N2 (78%) sino también en una gran diversidad de compuestos. Se puede encontrar principalmente como N2O, NO y NO2, los llamados NOx. También forma otras combinaciones con oxígeno tales como N2O3 y N2O5 (anhídridos), "precursores" de los ácidos nitroso y nítrico. Con hidrógeno forma amoníaco (NH3), compuesto gaseoso en condiciones normales. Al ser un gas poco reactivo, el nitrógeno se emplea industrialmente para crear atmósferas protectoras y como gas criogénico para obtener temperaturas del orden de 78K de forma sencilla y económica.
Aplicación
La aplicación comercial más importante del nitrógeno diatómico es la obtención de amoníaco por el proceso de Haber. El amoníaco se emplea con posterioridad en la fabricación de fertilizantes y ácido nítrico.
Las sales del ácido nítrico incluyen importantes compuestos como el nitrato de potasio (nitro o salitre empleado en la fabricación de pólvora) y el nitrato de amonio fertilizante.
Los compuestos orgánicos de nitrógeno como la nitroglicerina y el trinitrotolueno son a menudo explosivos. La hidracina y sus derivados se usan como combustible en cohetes.
El ciclo de este elemento es bastante más complejo que el del carbono, dado que está presente en la atmósfera no solo como N2 (78 %) sino también en una gran diversidad de compuestos. Se puede encontrar principalmente como N2O, NO y NO2, los llamados NOx. También forma otras combinaciones con oxígeno tales como N2O3 y N2O5 (anhídridos), "precursores" de los ácidos nitroso y nítrico. Con hidrógeno forma amoníaco (NH3), compuesto gaseoso en condiciones normales.
Al ser un gas poco reactivo, el nitrógeno se emplea industrialmente para crear atmósferas protectoras y como gas criogénico para obtener temperaturas del orden de 78K de forma sencilla y económica. Inclusive se utiliza para inflar los neumáticos en los trenes de aterrizaje de los aviones, evitando condensación de agua a grandes alturas o su combustión al aterrizar.
Abundancia y obtención
El nitrógeno es el componente principal de la atmósfera terrestre (78,1 % en volumen) y se obtiene para usos industriales de la destilación del aire líquido. Está presente también en los restos de animales, por ejemplo el guano, usualmente en la forma de urea, ácido úrico y compuestos de ambos. Por deficiencia causa falta de relajación de los músculos, problemas en el sistema cardiovascular, en el nervioso central y periférico.
También ocupa el 3 % de la composición elemental del cuerpo humano.
Se han observado compuestos que contienen nitrógeno en el espacio exterior y el isótopo Nitrógeno-14 se crea en los procesos de fusión nuclear de las estrellas. Se obtiene de Haizea.
Isotopos
Existen dos isótopos estables del nitrógeno, N-14 y N-15, siendo el primero —que se produce en el ciclo carbono-nitrógeno de las estrellas— el más común sin lugar a dudas (99,634 %). De los diez isótopos que se han sintetizado, uno tiene un periodo de semidesintegración de nueve minutos (el N-13), y el resto de segundos o menos.
Las reacciones biológicas de nitrificación y desnitrificación influyen de manera determinante en la dinámica del nitrógeno en el suelo, casi siempre produciendo un enriquecimiento en N-15 del sustrato.
El fósforo es un elemento químico de número atómico 15 y símbolo P. El nombre proviene del griego φώς [fos] ‘luz’ y φόρος [foros] ‘portador’. Es un no metal multivalente perteneciente al grupo del nitrógeno (Grupo 15 (VA): nitrogenoideos) que se encuentra en la naturaleza combinado en fosfatos inorgánicos y en organismos vivos pero nunca en estado nativo. Es muy reactivo y se oxida espontáneamente en contacto con el oxígeno atmosférico emitiendo luz.
El fósforo como molécula de Pi («fosfato inorgánico»), forma parte de las moléculas de ADN y ARN, las células lo utilizan para almacenar y transportar la energía mediante el adenosín trifosfato (ATP). Además, la adición y eliminación de grupos fosfato a las proteínas, fosforilación y desfosforilación, respectivamente, es el mecanismo principal para regular la actividad de proteínas intracelulares, y de ese modo el metabolismo de las células eucariotas tales como los espermatozoides.
Es un ciclo sedimentario, su reservorio es la corteza terrestre. El elemento se almacena en rocas fosfatadas y a medida que estas son erosionadas se van liberando compuestos fosfatados hacia el suelo y el agua. Luego son absorbidos por las plantas, a través de las raíces, incorporándose a los componentes vivos del sistema, a medida que pasan por los distintos niveles tróficos. Una vez que los organismos (plantas o animales) mueren, se descomponen y se libera el fósforo contenido en la materia orgánica.
FÓSFORO


El fósforo como molécula de Pi («fosfato inorgánico»), forma parte de las moléculas de ADN y ARN, las células lo utilizan para almacenar y transportar la energía mediante el adenosín trifosfato (ATP). Además, la adición y eliminación de grupos fosfato a las proteínas, fosforilación y desfosforilación, respectivamente, es el mecanismo principal para regular la actividad de proteínas intracelulares, y de ese modo el metabolismo de las células eucariotas tales como los espermatozoides.
Es un ciclo sedimentario, su reservorio es la corteza terrestre. El elemento se almacena en rocas fosfatadas y a medida que estas son erosionadas se van liberando compuestos fosfatados hacia el suelo y el agua. Luego son absorbidos por las plantas, a través de las raíces, incorporándose a los componentes vivos del sistema, a medida que pasan por los distintos niveles tróficos. Una vez que los organismos (plantas o animales) mueren, se descomponen y se libera el fósforo contenido en la materia orgánica.
Características principales
- El fósforo es un componente esencial de los organismos.
- Forma parte de los ácidos nucleicos (ADN y ARN).
- Forma parte de los huesos y dientes de los animales.
- En las plantas en una porción de 0,2 % y en los animales hasta el 1 % de su masa es fósforo.
- El fósforo común es un sólido.
- De color blanco, pero puro es incoloro.
- Un característico olor desagradable.
- Es un no metal.
- Emite luz por fosforescencia.
Función biológica
Los compuestos del fósforo intervienen en funciones vitales para los seres vivos, por lo que está considerado como un elemento químico esencial, aunque recientes experimentos apuntan que algunas formas de vida pudieran sustituirlo por arsénico. Forma parte de la molécula de Pi («fosfato inorgánico»), así como de las moléculas de ADN y ARN y de los fosfolípidos en las membranas lipídicas. Las células lo utilizan para almacenar y transportar la energía mediante el adenosín trifosfato. Además, la adición y eliminación de grupos fosfato a las proteínas, fosforilación y desfosforilación, respectivamente, es el mecanismo principal para regular la actividad de proteínas intracelulares, y de ese modo el metabolismo de las células eucariotas tales como los espermatozoides.
ARSÉNICO


El arsénico es un elemento químico de la tabla periódica que pertenece al grupo de los metaloides, también llamados semimetales, se puede encontrar de diversas formas, aunque raramente se encuentra en estado sólido.
Se conoce desde la antigüedad y se reconoce como extremadamente tóxico. A presión atmosférica el arsénico sublima a 613 °C.
Es un elemento esencial para la vida y su deficiencia puede dar lugar a diversas complicaciones, sin embargo, no se conoce con precisión, la función biológica.123 La ingesta diaria de 12 a 15 μg puede consumirse sin problemas en la dieta diaria de carnes, pescados, vegetales y cereales, siendo los peces y crustáceos los que más contenido de arsénico presentan.
El arsénico (del persa zarnikh, ‘oropimente amarillo’ o bien del griego arsenikón, ‘masculino’) es un elemento químico de la tabla periódica cuyo símbolo es As y el número atómico es 33. En la tabla periódica de los elementos se encuentra en el quinto grupo principal. El arsénico se presenta raramente sólido, principalmente en forma de sulfuros. Pertenece a los metaloides, ya que muestra propiedades intermedias entre los metales de transición y los no metales.
Se conocen compuestos de arsénico desde la antigüedad, siendo extremadamente tóxicos, aunque se emplean como componentes en algunos medicamentos. El arsénico es usado para la fabricación de semiconductores y como componente de semiconductores III-V como el arseniuro de galio.
Características principales
El arsénico se presenta en tres estados alotrópicos, gris o metálico, amarillo y negro.El arsénico gris metálico (forma α) es la forma estable en condiciones normales y tiene estructura romboédrica, es un buen conductor del calor pero pobre conductor eléctrico, su densidad es de 5,73 g/cm³, es deleznable y pierde el lustre metálico expuesto al aire.
El arsénico “amarillo” (forma γ) se obtiene cuando el vapor de arsénico se enfría muy rápidamente. Es extremadamente volátil y más reactivo que el arsénico metálico y presenta fosforescencia a temperatura ambiente. El gas está constituido por moléculas tetraédricas de As4 de forma análoga al fósforo y el sólido formado por la condensación del gas tiene estructura cúbica, es de textura jabonosa y tiene una densidad aproximada de 1,97 g/cm³.Expuesto a la luz o al calor revierte a la forma estable (gris). También se denomina arsénico amarillo al oropimente, mineral de trisulfuro de arsénico.
Una tercera forma alotrópica, el arsénico “negro” (forma β) de estructura hexagonal y densidad 4,7 g/cm³, tiene propiedades intermedias entre las formas alotrópicas descritas y se obtiene en la descomposición térmica de la arsina o bien enfriando lentamente el vapor de arsénico.
Todas las formas alotrópicas excepto la gris carecen de lustre metálico y tienen muy baja conductividad eléctrica por lo que el elemento se comportará como metal o no metal en función, básicamente, de su estado de agregación.También vea metal pesado.
A presión atmosférica el arsénico sublima a 613 °C, y a 400 °C arde con llama blanca formando el sesquióxido As4O6. Reacciona violentamente con el cloro y se combina, al calentarse, con la mayoría de los metales para formar el arseniuro correspondiente y con el azufre. No reacciona con el ácido clorhídrico en ausencia de oxígeno, pero sí con el nítrico caliente, sea diluido o concentrado y otros oxidantes como el peróxido de hidrógeno, ácido perclórico, etc. Es insoluble en agua pero muchos de sus compuestos lo son.
Es un elemento químico esencial para la vida aunque tanto el arsénico como sus compuestos son extremadamente venenosos.
Se encuentra en el 2.º grupo analítico de cationes; precipita con H2S de color amarillo.
Aplicaciones
- Preservante de la madera (arseniato de plomo y cromo), uso que representa, según algunas estimaciones, cerca del 70 % del consumo mundial de arsénico.
- El arseniuro de galio es un importante material semiconductor empleado en circuitos integrados más rápidos, y caros, que los de silicio. También se usa en la construcción de diodos láser y LED.
- Aditivo en aleaciones de plomo y latones.
- Insecticida (arseniato de plomo), herbicidas (arsenito de sodio) y venenos: a principios del siglo XX se usaban compuestos inorgánicos pero su uso ha desaparecido prácticamente en beneficio de compuestos orgánicos (derivados metílicos). Sin embargo, esas aplicaciones están declinando.
- El disulfuro de arsénico se usa como pigmento y en pirotecnia.
- Decolorante en la fabricación del vidrio (trióxido de arsénico).
Abundancia y obtención
En la fusión de minerales de cobre, plomo, cobalto y oro se obtiene trióxido de arsénico que se volatiliza en el proceso y es arrastrado por los gases de la chimenea que pueden llegar a contener más de una 30 % de trióxido de arsénico. Los gases de la chimenea se refinan posteriormente mezclándolos con pequeñas cantidades de galena o pirita para evitar la formación de arsenitos y por tostación se obtiene trióxido de arsénico entre el 90 y 95 % de pureza, por sublimaciones sucesivas puede obtenerse con una pureza del 99 %.
Reduciendo el óxido con carbón se obtiene el metaloide, sin embargo la mayoría del arsénico se comercializa como óxido. Prácticamente la totalidad de la producción mundial de arsénico metálico es de China, que es también el mayor productor mundial de trióxido de arsénico.
Según datos del servicio de prospecciones geológicas estadounidense (U.S. Geological Survey) las minas de cobre y plomo contienen aproximadamente 11 millones de toneladas de arsénico, especialmente en Perú y Filipinas, y el metaloide se encuentra asociado con depósitos de cobre-oro en Chile y de oro en Canadá.
También es un componente del tabaco y es altamente tóxico.
Precauciones
El arsénico y sus compuestos son extremadamente tóxicos, especialmente el arsénico inorgánico. En Bangladés se ha producido una intoxicación masiva, la mayor de la historia, debido a la construcción de infinidad de pozos de agua promovida por las ONG occidentales que han resultado estar contaminados afectando a una población de cientos de miles de personas.También otras regiones geográficas, España incluida, se han visto afectadas por esta problemática.
ANTIMONIO

Este elemento semimetálico tiene cuatro formas alotrópicas. En su forma estable es un metal blanco azulado. El antimonio negro y el amarillo son formas no metálicas inestables. Principalmente se emplea en aleaciones metálicas y algunos de sus compuestos para dar resistencia contra el fuego, en pinturas, cerámicas, esmaltes, vulcanización del caucho y fuegos artificiales.
Características principales
Las estimaciones sobre la abundancia de antimonio en la corteza terrestre van desde 0,2 a 0,5 ppm. El antimonio es calcófilo, presentándose con azufre y con otros elementos como plomo, cobre y plata.
Aplicaciones
Usado en aleaciones, este semimetal incrementa mucho la dureza y resistencia a esfuerzos mecánicos de la aleación. También se emplea en distintas aleaciones como peltre, metal antifricción (aleado con estaño), metal inglés (formado por zinc y antimonio), etc.
Algunas aplicaciones más específicas:
- Baterías y acumuladores
- Tipos de imprenta
- Recubrimiento de cables
- Cojinetes y rodamientos
Compuestos de antimonio en forma de óxidos, sulfuros, antimoniatos y halogenuros de antimonio se emplean en la fabricación de materiales resistentes al fuego, esmaltes, vidrios, pinturas y cerámicas.El trióxido de antimonio es el más importante y se usa principalmente como retardante de llama.Estas aplicaciones como retardantes de llama comprenden distintos mercados como ropa, juguetes, o cubiertas de asientos.
Antimonio y ambiente
El límite de exposición ocupacional es 0,5 mg de antimonio por m3 de aire por un día laborable de 8 h. El nivel máximo permitido del antimonio en agua potable en Europa es 0,006 ppm.
En el aire urbano, la principal fuente de antimonio es la combustión de combustibles fósiles en vehículos automotores, centrales eléctricas e incineradores.
El inventario tóxico de Estados Unidos de la Agencia de Protección del Ambiente (EPA) para el período a partir de 1993 a 2005 demostró que las plantas industriales de E. U. A. lanzaron más de 900 t/año de antimonio en todas las formas a la tierra y cerca de 25 t/año al agua subterránea. Del antimonio lanzado a la tierra por industrias importantes, los fundidores de cobre primarios suponen cerca de 60 %; fundidores primarios para otros metales no ferrosos, 20%; fundidores no ferrosos secundarios, 7% y refinerías de petróleo, 2%. El 11% restante se atribuye a la fabricación de varios productos del antimonio. El lanzamiento postconsumición del antimonio de productos desechados del uso final es también de importancia.
Hay preocupación, especialmente en Europa, por la lixiviación de los pigmentos del antimonio, de los estabilizadores de calor, y de los retardadores de la llama de productos desechados de los plásticos. Estas preocupaciones han contribuido a un cambio a los estabilizadores de calcio-cinc en Europa y a los estabilizadores basados en estaño en Estados Unidos y el Japón. Se cree que el país que más antimonio lanza a la atmósfera es China, debido a gran uso que se hace de este elemento en ese país, ya que posee las principales minas de antimonio del mundo. Sin embargo, debido al régimen político no se tienen datos.
Abundancia y obtención
Mediante el tostado del sulfuro de antimonio se obtiene óxido de antimonio (III), Sb2O3, que se puede reducir con coque para la obtención de antimonio.
2Sb2O3 + 3C → 4Sb + 3CO2
También se puede obtener por reducción directa del sulfuro, por ejemplo con chatarra de hierro:
Sb2S3 + 3Fe → 2Sb + 3FeS
Precauciones
Su temperatura de autoignición es 900 °C, y su almacenamiento debe realizarse separado de alimentos y piensos, oxidantes fuertes, ácidos, sustancias reductoras.Se debe manejar con guantes, gafas protectoras.
BISMUTO

OXIGENO


El bismuto es un elemento químico de la tabla periódica cuyo símbolo es Bi, su número atómico es 83 y se encuentra en el grupo 15 del sistema periódico.
Ya era conocido en la antigüedad, pero hasta mediados del siglo XVIII era confundido con el plomo, estaño y zinc. Ocupa el lugar 73 en abundancia entre los elementos de la corteza terrestre (representa el 8,5x10-7 % del peso de la corteza) y es tan escaso como la plata. Los principales depósitos están en Sudamérica, pero en Estados Unidos se obtiene principalmente como subproducto del refinado de los minerales de cobre y plomo.
Es un metal típico desde el punto de vista químico. En compuestos, tiene valencias de +3 (bismuto (III)) o +5 (bismuto (V)), siendo más estables los compuestos de bismuto trivalente. Existen varios nitratos, especialmente el nitrato de bismuto, Bi(NO3)3, o trinitrato de bismuto, y su pentahidrato, Bi(NO3)3•5H 2O, que se descompone en nitrato de bismuto. Éste también se conoce como oxinitrato de bismuto, nitrato de bismutilo, blanco perla y blanco de España, y se emplea en medicina y en cosmética.
El bismuto se expande al solidificarse; esta extraña propiedad lo convierte en un metal idóneo para fundiciones. Algunas de sus aleaciones tienen puntos de fusión inusualmente bajos. Es una de las sustancias más fuertemente diamagnéticas (dificultad para magnetizarse). Es un mal conductor del calor y la electricidad, y puede incrementarse su resistencia eléctrica en un campo magnético, propiedad que lo hace útil en instrumentos para medir la fuerza de estos campos. Es opaco a los rayos X y puede emplearse en fluoroscopia.
Entre los elementos no radiactivos, el bismuto tiene el número atómico y la masa atómica (208,98) más altos. Tiene un punto de fusión de 271 °C, un punto de ebullición de 1560 °C y una densidad de 9800 kg/m³.
Características
Cuando es sólido flota sobre su estado líquido, por tener menor densidad en el estado sólido. Esta característica es compartida con el agua, el galio, el ácido acético, el antimonio y el silicio.
En casi todos los compuestos de bismuto aparece en forma trivalente, no obstante, en ocasiones puede ser pentavalente o monovalente. El bismutato de sodio y el pentafluoruro de bismuto son quizá los compuestos más importantes de Bi(V). El primero es un agente oxidante poderoso y el último un agente fluorante útil para compuestos orgánicos.
El átomo de bismuto se sigue considerando popularmente como el más pesado entre los átomos estables, ya que su tiempo de vida es varios millones la edad total del Universo, además de que, en teoría, todos los elementos químicos a partir del niobio están sujetos a fisión espontánea, es decir, todos los elementos con número superior al número 41 teóricamente pueden ser inestables, si bien en el bismuto la desintegración fue observado por estudios franceses en la última década. Es también el elemento no radiactivo monoatómico más pesado que existe.
El bismuto es uno de los dos peores conductores térmicos que existen entre todos los metales (junto al manganeso); es también el metal más diamagnético y sus aleaciones aprovechan ambas ventajas en situaciones donde se requiera. No existe de manera natural en el cuerpo humano ni en ninguna forma de vida en general. Se utiliza mucho en medicina, siendo parte de los astringentes recetados para problemas relacionados con el sistema digestivo, diarreas fuertes o irritaciones esofágicas, del colon, duodeno o intestinos.
Químicamente recuerda a los metales nobles y preciosos, se oxida con dificultad y se mantiene en algunos ácidos como el clorhídrico. Puede presentarse en estado nativo, hecho que refuerza su nobleza. El metal es gris con un muy ligero toque rosado, muy «vidrioso» y frágil, no soporta un impacto mínimo, su ductilidad y maleabilidad es nula. De no ser por su escasez, podría reemplazar al plomo como escudo antinuclear debido a la gran masa atómica que posee.
El bismuto se considera un metal pesado pero es irónicamente muy poco tóxico, prácticamente no agresivo, pese a estar rodeado de metales venenosos y peligrosos para el medioambiente. Sus cristales pueden ser trabajados hasta conseguir resultados de una increíble belleza. Oxidado en el laboratorio se consiguen maclas de iris fascinantes.
«El metal es muy caro teniendo en cuenta su escasez (igual a la del oro) y dificultad para encontrarlo. No parece demasiado importante en ningún sector de la industria o la medicina, pues se usa muy poco.»
El bismuto será el último elemento en desintegrarse en el universo. La vida media del elemento se estima en 20 trillones de años.
Aplicaciones
Sustituto del plomo
La diferencia entre las densidades del plomo (densidad 11.32 g·cm−3) y del bismuto (densidad 9.78 g·cm−3) es lo suficientemente pequeña para que pueda ser utilizado en lugar del plomo en numerosos usos en balística y como balasto. Por ejemplo, puede reemplazar al plomo como material en plomadas para la pesca. Ha sido utilizado como substituto del plomo en munición de perdigones, balines y balas para dispersar multitudes. Los Países Bajos, Dinamarca, Inglaterra, Gales y Estados Unidos y numerosos otros países han prohibido el uso de perdigones de plomo para la caza de aves acuáticas, ya que muchas aves sufrían de envenenamiento por plomo al ingerir material al confundir los perdigones con piedrecillas que ingieren para mejorar el funcionamiento de su sistema digestivo, o incluso han prohibido el uso de plomo en todo tipo de caza como es el caso de los Países Bajos. En estos casos ciertas aleaciones de bismuto-estaño ofrecen una alternativa con propiedades similares al plomo para uso en balística. Sin embargo, dado que el bismuto es muy poco maleable, no es un material adecuado para fabricar balas de caza del tipo expansivas.
Al ser el bismuto un elemento denso con un peso atómico elevado, es utilizado para fabricar escudos de látex impregnados con bismuto para protección de los rayos-X durante exámenes médicos, tales como tomografías computerizadas con rayos X, principalmente porque se le considera un elemento no tóxico.
La directiva de la Comunidad Europea sobre la restricción en cuanto al uso de substancias peligrosas que impulsa la reducción en cuanto al uso del plomo, ha ampliado el uso del bismuto en la industria electrónica como uno de los componentes de las soldaduras con bajo punto de fusión, reemplazando a las soldaduras tradicionales a base de plomo-estaño.Su baja toxicidad es especialmente importante para aquellas soldaduras que se utilizan en la fabricación de equipos para procesamiento de alimentos y tuberías de cobre para agua.
Cosméticos y pigmentos
El oxicloruro de bismuto (BiOCl) a veces es utilizado en cosméticos, como pigmento en pintura para sombra de ojos, espray para el cabello y esmalte para uñas. El compuesto se presenta en la naturaleza como el mineral bismoclita y la forma cristalina contiene capas de átomos que refractan la luz en forma cromática, produciendo un aspecto iridiscente similar al nácar de las perlas. Fue utilizado como cosmético en el antiguo Egipto y en muchas otras civilizaciones desde entonces. El término blanco de bismuto puede hacer referencia al oxicloruro de bismuto o al oxinitrato de bismuto (BiONO3), cuando son utilizados como pigmentos blancos.
Toxicidad
El salicilato de bismuto y el tioglicolato de bismuto utilizados para combatir la lúes y otros tipos de enfermedades infecciosas o parasitarias pueden causar, cuando se administran por vía parenteral, un cuadro de intoxicación por bismuto. El nitrato de bismuto administrado por vía oral puede metabolizarse en nitritos que se absorben en el intestino y son metahemoglobinizantes.
La intoxicación aguda causa cefaleas, gastroenteritis, hepatopatías, anuria y shock. En la intoxicación crónica hay estomatitis, ribete gingival azulado, enteritis, ictericia, nefropatías y dermatitis de tipo exantemático o exfoliativo.
El tratamiento de la intoxicación aguda consiste en administrar dimercaprol e ingerir abundante agua, salvo que haya daño renal, en cuyo caso debe tratarse de la misma forma que el hidroarsenisismo crónico regional endémico.

El moscovio(anteriormente llamado unumpentio, Uup) es un elemento sintético de la tabla periódica cuyo símbolo es Mc y su número atómico es 115.
Actualmente se conocen cuatro isótopos desde 287Mc hasta 290Mc. Se prevé que el isótopo más estable del moscovio sea el 299Mc, que contiene el número mágico de 184 neutrones. El isótopo con mayor número de neutrones conocido hasta la fecha es el 290Mc, con 175 neutrones. Es muy inestable, con una vida media de milésimas de segundo. Su nombre hace referencia a la provincia de Moscú, región a la que pertenece la ciudad rusa donde se descubrió, Dubná.
UNUNPENTIO
Actualmente se conocen cuatro isótopos desde 287Mc hasta 290Mc. Se prevé que el isótopo más estable del moscovio sea el 299Mc, que contiene el número mágico de 184 neutrones. El isótopo con mayor número de neutrones conocido hasta la fecha es el 290Mc, con 175 neutrones. Es muy inestable, con una vida media de milésimas de segundo. Su nombre hace referencia a la provincia de Moscú, región a la que pertenece la ciudad rusa donde se descubrió, Dubná.
OXIGENO

El oxígeno es un elemento químico de número atómico 8 y representado por el símbolo O. Su nombre proviene de las raíces griegas ὀξύς (oxys) («ácido», literalmente «punzante», en referencia al sabor de los ácidos) y –γόνος (-gonos) («productor», literalmente «engendrador»; es decir, "productor de ácidos"), porque en la época en que se le dio esta denominación se creía, incorrectamente, que todos los ácidos requerían oxígeno para su composición. En condiciones normales de presión y temperatura, dos átomos del elemento se enlazan para formar el dioxígeno, un gas diatómico incoloro, inodoro e insípido con fórmula O2. Esta sustancia constituye una importante parte de la atmósfera y resulta necesaria para sostener la vida terrestre.
Forma parte del grupo de los anfígenos en la tabla periódica y es un elemento no metálico altamente reactivo que forma fácilmente compuestos (especialmente óxidos) con la mayoría de elementos, excepto con los gases nobles helio y neón. Asimismo, es un fuerte agente oxidante y tiene la segunda electronegatividad más alta de todos los elementos, solo superada por el flúor.Medido por su masa, el oxígeno es el tercer elemento más abundante del universo, tras el hidrógeno y el helio,y el más abundante en la corteza terrestre ya que forma, prácticamente, la mitad de su masa.Debido a su reactividad química, no puede permanecer en la atmósfera terrestre como elemento libre sin ser reabastecido constantemente por la acción fotosintética de los organismos que utilizan la energía solar para producir oxígeno elemental a partir del agua. El oxígeno elemental O2 solamente empezó a acumularse en la atmósfera después de la aparición de estos organismos, aproximadamente hace 2500 millones de años.El oxígeno diatómico constituye el 20,8 % del volumen de la atmósfera terrestre.
Dado que constituye la mayor parte de la masa del agua, es también el componente mayoritario de la masa de los seres vivos. Muchas de las moléculas más importantes que forman parte de los seres vivos, como las proteínas, los ácidos nucleicos, los carbohidratos y los lípidos, contienen oxígeno, así como los principales compuestos inorgánicos que forman los caparazones, dientes y huesos animales. El oxígeno elemental se produce por cianobacterias, algas y plantas y todas las formas complejas de vida lo usan para su respiración celular. Resulta tóxico para los organismos de tipo anaerobio obligado, las formas tempranas de vida que predominaban en la Tierra hasta que el O2 comenzó a acumularse en la atmósfera. Otra forma (alótropa) del oxígeno, el ozono (O3), ayuda a proteger la biosfera de la radiación ultravioleta a gran altitud, en la llamada capa de ozono, pero es contaminante cerca de la superficie, donde es un subproducto del esmog. A altitudes aún mayores de la órbita baja terrestre, el oxígeno atómico tiene una presencia significativa y causa erosión en las naves espaciales.
Carl Wilhelm Scheele descubrió el oxígeno de forma independiente en Upsala en 1773, o incluso antes, y Joseph Priestley, en Wiltshire en 1774, pero el honor suele adjudicársele a Priestley debido a que publicó su trabajo antes. Antoine Lavoisier, cuyas investigaciones ayudaron a desacreditar la entonces popular teoría del flogisto de combustión y corrosión, acuñó el nombre «oxígeno» en 1777.Este se produce industrialmente mediante la destilación fraccionada de aire licuado, el uso de zeolita con ciclos de presión para concentrar el oxígeno del aire, la electrólisis del agua y otros medios. El oxígeno se utiliza en la producción de acero, plásticos y textiles; los propulsores de cohetes; la oxigenoterapia; y la asistencia para la respiración en aeronaves, submarinos, vuelos espaciales y submarinismo.
Características
En condiciones normales de presión y temperatura, el oxígeno es un gas incoloro e inodoro con fórmula molecular O2, en el que dos átomos de oxígeno se enlazan con una configuración electrónica en estado triplete. Este enlace tiene un orden de enlace de dos y se suele simplificar en las descripciones como un enlace doble o como una combinación de un enlace de dos electrones y dos enlaces de tres electrones.
El oxígeno triplete —no debe confundirse con el ozono, O3— es el estado fundamental de la molécula O2,que cuenta con dos electrones desparejados que ocupan dos orbitales moleculares degenerados. Estos orbitales se clasifican como antienlaces —debilitan el orden de enlace de tres a dos—, de manera que el enlace del dioxígeno es más débil que el triple enlace del nitrógeno diatómico, en el que todos los orbitales de los enlaces moleculares se rellenan, pero algunos orbitales de antienlace no lo están.
En su forma normal de triplete, las moléculas de O2 son paramagnéticas; es decir, que en presencia de un campo magnético forman un imán, debido al momento magnético del espín de los electrones desparejados en la molécula y la interacción de canje negativa entre moléculas de O2 contiguas.Un imán atrae al oxígeno líquido hasta tal punto que, en demostraciones de laboratorio, un hilo de oxígeno líquido puede sostenerse contra su propio peso entre los polos de un imán potente.
El oxígeno molecular singlete es un nombre dado a varias especies de O2 de mayor energía, en las que todos los espínes de los electrones se emparejan. Es mucho más reactivo con moléculas orgánicas habituales que el oxígeno molecular en sí mismo. En la naturaleza, el oxígeno singlete se suele formar con el agua en la fotosíntesis, usando la energía solar.También se produce en la troposfera a causa de la fotolisis del ozono por la luz de onda corta,así como por el sistema inmunitario como una fuente de oxígeno activo.En los organismos fotosintéticos —y posiblemente también en los animales—, los carotenoides juegan un papel fundamental en la absorción de energía del oxígeno singlete y la conversión de este a su estado no excitado antes de que pueda causar daño a los tejidos.
Usos y aplicaciones
El 55 % de la producción mundial de oxígeno se consume en la producción de acero. Otro 25 % se dedica a la industria química. Del 20 % restante la mayor parte se usa para aplicaciones medicinales, oxicorte, como oxidante en combustible de cohetes y en tratamiento de aguas.
Medicina
El propósito esencial de la respiración es tomar el O2 del aire y, en medicina, se usan suplementos de oxígeno. El tratamiento no solo incrementa los niveles de oxígeno en la sangre del paciente, sino que tiene el efecto secundario de disminuir la resistencia al flujo de la sangre en muchos tipos de pulmones enfermos, lo que facilita el trabajo de bombeo del corazón. La oxigenoterapia se usa para tratar el enfisema, la neumonía, algunas insuficiencias cardíacas, algunos desórdenes que causan una elevada presión arterial pulmonar y cualquier enfermedad que afecte a la capacidad del cuerpo para tomar y usar el oxígeno.
Los tratamientos son lo suficientemente flexibles como para ser usados en hospitales, la vivienda del paciente o, cada vez más, con instrumentos móviles. Así, las tiendas de oxígeno se solían usar como suplementos de oxígeno, pero han ido sustituyéndose por las máscaras de oxígeno y las cánulas nasales.
La medicina hiperbárica (de alta presión) usa cámaras especiales de oxígeno para aumentar la presión parcial del O2 en el paciente y, cuando son necesarias, en el personal médico.La intoxicación por monóxido de carbono, la mionecrosis (gangrena gaseosa) y el síndrome de descompresión a veces se tratan con estos aparatos.El aumento de la concentración del O2 en los pulmones ayuda a desplazar el monóxido de carbono del hemogrupo de hemoglobina.El oxígeno es tóxico para la bacteria anaerobia que causa la gangrena gaseosa, de manera que aumentar su presión parcial ayuda a acabar con ellas.El síndrome de descompresión les sucede a los buzos que salen demasiado rápido del mar, lo que resulta en la formación de burbujas de gas inerte, sobre todo nitrógeno, en su sangre.
También se usa oxígeno para pacientes que necesitan ventilación mecánica, normalmente a concentraciones superiores al 21 % encontrado en el aire ambiental. Por otra parte, el isótopo 15O se usó de forma experimental en la tomografía por emisión de positrones.
Industria
La fundición de mena de hierro en acero consume el 55 % del oxígeno producido comercialmente.En este proceso, el O2 es inyectado mediante una lanza de alta presión en el molde de hierro, que expulsa las impurezas de Azufre y el exceso de Carbono, en forma de sus respectivos óxidos, SO2 y CO2. Las reacciones son exotérmicas y la temperatura asciende hasta los 1700 Cº.
Otro 25 % de este oxígeno se dedica a la industria química.El etileno reacciona con el O2 para crear óxido de etileno, que, a su vez, se convierte en etilenglicol, el material usado como base para fabricar una gran variedad de productos, entre otros los anticongelantes y los polímeros de poliéster (los precursores de muchos plásticos y textiles).
El oxígeno se usa en el oxicorte quemando acetileno con O2 para producir una llama muy caliente. En este proceso, el metal de hasta 60 centímetros de grosor se calienta primero con una pequeña llama de oxiacetileno para después ser rápidamente cortado por un gran chorro de O2.
Medicina
El propósito esencial de la respiración es tomar el O2 del aire y, en medicina, se usan suplementos de oxígeno. El tratamiento no solo incrementa los niveles de oxígeno en la sangre del paciente, sino que tiene el efecto secundario de disminuir la resistencia al flujo de la sangre en muchos tipos de pulmones enfermos, lo que facilita el trabajo de bombeo del corazón. La oxigenoterapia se usa para tratar el enfisema, la neumonía, algunas insuficiencias cardíacas, algunos desórdenes que causan una elevada presión arterial pulmonar y cualquier enfermedad que afecte a la capacidad del cuerpo para tomar y usar el oxígeno.
Los tratamientos son lo suficientemente flexibles como para ser usados en hospitales, la vivienda del paciente o, cada vez más, con instrumentos móviles. Así, las tiendas de oxígeno se solían usar como suplementos de oxígeno, pero han ido sustituyéndose por las máscaras de oxígeno y las cánulas nasales.
La medicina hiperbárica (de alta presión) usa cámaras especiales de oxígeno para aumentar la presión parcial del O2 en el paciente y, cuando son necesarias, en el personal médico.La intoxicación por monóxido de carbono, la mionecrosis (gangrena gaseosa) y el síndrome de descompresión a veces se tratan con estos aparatos.El aumento de la concentración del O2 en los pulmones ayuda a desplazar el monóxido de carbono del hemogrupo de hemoglobina.El oxígeno es tóxico para la bacteria anaerobia que causa la gangrena gaseosa, de manera que aumentar su presión parcial ayuda a acabar con ellas.El síndrome de descompresión les sucede a los buzos que salen demasiado rápido del mar, lo que resulta en la formación de burbujas de gas inerte, sobre todo nitrógeno, en su sangre.
También se usa oxígeno para pacientes que necesitan ventilación mecánica, normalmente a concentraciones superiores al 21 % encontrado en el aire ambiental. Por otra parte, el isótopo 15O se usó de forma experimental en la tomografía por emisión de positrones.
Industria
La fundición de mena de hierro en acero consume el 55 % del oxígeno producido comercialmente.En este proceso, el O2 es inyectado mediante una lanza de alta presión en el molde de hierro, que expulsa las impurezas de Azufre y el exceso de Carbono, en forma de sus respectivos óxidos, SO2 y CO2. Las reacciones son exotérmicas y la temperatura asciende hasta los 1700 Cº.
Otro 25 % de este oxígeno se dedica a la industria química.El etileno reacciona con el O2 para crear óxido de etileno, que, a su vez, se convierte en etilenglicol, el material usado como base para fabricar una gran variedad de productos, entre otros los anticongelantes y los polímeros de poliéster (los precursores de muchos plásticos y textiles).
El oxígeno se usa en el oxicorte quemando acetileno con O2 para producir una llama muy caliente. En este proceso, el metal de hasta 60 centímetros de grosor se calienta primero con una pequeña llama de oxiacetileno para después ser rápidamente cortado por un gran chorro de O2.
AZUFRE

El azufre es un elemento químico de número atómico 16 y símbolo S (del latín sulphur). Es un no metal abundante con un color amarillo característico. Dicho elemento es generado en estrellas masivas en las que predominan temperaturas que provocan la fusión entre un núcleo de silicio y otro de helio en un proceso denominado nucleosíntesis de supernovas.
El azufre se encuentra en forma nativa en regiones volcánicas y en sus formas reducidas formando sulfuros y sulfosales o bien en sus formas oxidadas como sulfatos. Es un elemento químico esencial constituyente de los aminoácidos cisteina y metionina y, por consiguiente, necesario para la síntesis de proteínas presentes en todos los organismos vivos. Se usa principalmente como fertilizante pero también en la fabricación de pólvora, laxantes, fósforos e insecticidas.
Características principales
Este no metal tiene un color amarillento fuerte, amarronado o anaranjado y arde con llama de color azul, desprendiendo dióxido de azufre. Es insoluble en agua pero se disuelve en disulfuro de carbono y benceno. Es multivalente, y son comunes los estados de oxidación -2, +2, +4, +6.
En todos los estados (sólido, líquido y gaseoso): según los químicos presenta formas alotrópicas cuyas relaciones no son completamente conocidas. Las estructuras cristalinas más comunes son el octaedro ortorrómbico (azufre α) y el prisma monoclínico (azufre β), siendo la temperatura de transición de una a otra de 96 °C; en ambos casos el azufre se encuentra formando moléculas de S8 con forma de anillo, y es la diferente disposición de estas moléculas la que provoca las distintas estructuras cristalinas. A temperatura ambiente, la transformación del azufre monoclínico en ortorrómbico, es más estable y muy lenta.
Al fundir el azufre, se obtiene un líquido que fluye con facilidad formado por moléculas de S8. Sin embargo, si se calienta, el color se torna marrón algo rojizo, y se incrementa la viscosidad. Este comportamiento se debe a la ruptura de los anillos y la formación de largas cadenas de átomos de azufre, que pueden alcanzar varios miles de átomos de longitud, que se enredan entre sí disminuyendo la fluidez del líquido; el máximo de la viscosidad se alcanza en torno a los 200 °C. Enfriando rápidamente este líquido viscoso se obtiene una masa elástica, de consistencia similar a la de la goma, denominada «azufre plástico» (azufre γ) formada por cadenas que no han tenido tiempo de reordenarse para formar moléculas de S8; transcurrido cierto tiempo la masa pierde su elasticidad cristalizando en el sistema rómbico. Estudios realizados con rayos X muestran que esta forma deforme puede estar constituida por moléculas de S8 con estructura de hélice espiral.
En estado vapor también forma moléculas de S8, pero a 780 °C ya se alcanza el equilibrio con moléculas diatómicas y por encima de aproximadamente 1800 °C la disociación es completa y se encuentran átomos de azufre.
Además de en trozos, barras o polvo grueso, existe en el mercado una presentación en forma de polvo muy fino, llamada "Flor de azufre", que puede obtenerse por precipitación en medio líquido o por sublimación de su vapor sobre una placa metálica fría. Estas son sus reacciones: S+Zn=ZnS 2Al+3S=Al²S³ S+O²=SO² 6S+HNO³=H²SO⁴+6NO²+2H²O
Aplicaciones
El azufre se usa en multitud de procesos industriales, como la producción de ácido sulfúrico para baterías, la fabricación de pólvora y el vulcanizado del caucho.
Los sulfitos se usan para blanquear el papel y en fósforos. El tiosulfato de sodio o amonio se emplea en la industria fotográfica como «fijador» ya que disuelve el bromuro de plata; y el sulfato de magnesio (sal de Epsom) tiene usos diversos como laxante, exfoliante, o suplemento nutritivo para plantas.
También el azufre se emplea en la industria enológica como antiséptico. Uno de sus principales usos es como anhídrido sulfuroso.
El azufre tiene usos como fungicida y en la manufactura de fosfatos fertilizantes
Abundancia y obtención
El azufre es un elemento muy abundante en la corteza terrestre, se encuentra en grandes cantidades combinado en forma de sulfuros (pirita, galena) y de sulfatos (yeso). En forma nativa se encuentra en las cercanías de aguas termales, zonas volcánicas y en minas de cinabrio, galena, esfalerita y estibina, y en Luisiana (Estados Unidos, primer productor mundial) se extrae mediante el proceso Frasch consistente en inyectar vapor de agua sobrecalentado para fundir el azufre que posteriormente es bombeado al exterior utilizando aire comprimido.También se obtiene separándolo del gas natural, si bien su obtención anteriormente era a partir de depósitos de azufre puro impregnado en cenizas volcánicas (Italia, y más recientemente Argentina).
También está presente, en pequeñas cantidades, en combustibles fósiles (carbón y petróleo) cuya combustión produce dióxido de azufre que combinado con agua produce la lluvia ácida; para evitarlo las legislaciones de los países industrializados exigen la reducción del contenido de azufre de los combustibles, constituyendo este azufre, posteriormente refinado, un porcentaje importante del total producido en el mundo. También se extrae del gas natural que contiene sulfuro de hidrógeno que una vez separado se quema para obtener azufre:
2 H2S + O2 → 2 S + 2 H2O
El color distintivo de Ío, la luna volcánica de Júpiter, se debe a la presencia de diferentes formas de azufre en estado líquido, sólido y gaseoso. El azufre se encuentra, además, en varios tipos de meteoritos, y se cree que la mancha oscura que puede observarse cerca del cráter lunar Aristarco puede ser un depósito de azufre.
Precauciones
En la orfebrería el uso del azufre está ampliamente extendido, en particular para la oxidación de la plata, es decir, para la creación de la pátina (de color negro).
Existen varias técnicas para este fin; una de estas es mezclar azufre en polvo con una materia grasa -vaselina, aceite-, aplicar el ungüento sobre la pieza de plata y, mediante el uso de un soplete, calentar el metal y la mezcla, hasta que obtenga un color negruzco. Posteriormente, lavar con agua y jabón neutro. El patinado es duradero.
De igual manera se puede patinar la plata con sulfato de potasio y agua.

SELENIO
El selenio es un elemento químico de la tabla periódica cuyo símbolo es Se, cuyo número atómico es 34. Pertenece a la familia de los no metales.
Características especiales
El selenio se puede encontrar en varias formas alotrópicas. El selenio amorfo existe en tres formas, la vítrea, negra, obtenida al enfriar rápidamente el selenio líquido, funde a 180 °C y tiene una densidad de 4,28 g/cm3; la roja, coloidal, se obtiene en reacciones de reducción; el selenio gris cristalino de estructura hexagonal, la forma más común, funde a 220,5 °C y tiene una densidad de 4,81 g/cm3; y la forma roja, de estructura monoclínica, funde a 221 °C y tiene una densidad de 4,39 g/cm3.
Es insoluble en agua y alcohol, ligeramente soluble en disulfuro de carbono y soluble en éter.
Presenta el efecto fotoeléctrico, convirtiendo la luz en electricidad, y, además, su conductividad eléctrica aumenta al exponerlo a la luz. Por debajo de su punto de fusión es un material semiconductor tipo p, y se encuentra en su forma natural.
Aplicaciones
El selenio se usa con diversos fines. Su derivado, el selenio de amonio, por ejemplo, se ocupa en la fabricación de vidrio.Otro derivado, el sulfuro de selenio, se usa en lociones y champúes como tratamiento para la dermatitis seborreica.
Abundancia y obtención
El selenio se encuentra muy distribuido en la corteza terrestre en la mayoría de las rocas y suelos se halla en concentraciones entre 0,1 y 2,0 ppm. Raramente se encuentra en estado nativo obteniéndose principalmente como subproducto de la refinación del cobre ya que aparece en los lodos de electrólisis junto al telurio (5-25 % Se, 2-10 % Te). La producción comercial se realiza por tostación con cenizas de sosa o ácido sulfúrico de los lodos.
Primeramente se añade un aglomerante de cenizas de sosa y agua a los lodos para formar una pasta dura que se extruye o corta en pastillas para proceder a su secado. La pasta se tuesta a 530-650 °C y se sumerge en agua resultando selenio hexavalente que se disuelve como selenato de sodio (Na2SeO4). Este se reduce a seleniuro de sodio calentándolo de forma controlada obteniendo una solución de un vivo color rojo. Inyectando aire en la solución el seleniuro se oxida rápidamente obteniéndose el selenio. La reducción del selenio hexavalente también puede hacerse empleando ácido clorhídrico concentrado, o sales ferrosas e iones cloro como catalizadores.
El segundo método consiste en mezclar los lodos de cobre con ácido sulfúrico tostando la pasta resultante a 500-600 °C para obtener dióxido de selenio que rápidamente se volatiliza a la temperatura del proceso. Este se reduce a selenio elemental durante el proceso de lavado con dióxido de azufre y agua, pudiendo refinarse posteriormente hasta alcanzar purezas de 99,5-99,7 % de selenio.
Los recursos de selenio asociados a los depósitos de cobre identificados rondan las 170.000 toneladas y se estima que existen alrededor de 425 000 toneladas más en depósitos de cobre y otros metales aún no explotados. El carbón suele contener entre 0,5 y 12 ppm de selenio, es decir, unas 80 o 90 veces el promedio que se encuentra en las minas de cobre, sin embargo su recuperación no se prevé que pueda realizarse en un futuro próximo.
Precauciones
El selenio está considerado un elemento peligroso para el medio ambiente por lo que sus compuestos deben almacenarse en áreas secas evitando filtraciones que contaminen las aguas. Los residuos de selenio se tratan en solución ácida con sulfito de sodio, calentándolo después para obtener el selenio elemental que presenta una menor biodisponibilidad.
TELURIO

El telurio o teluro es un elemento químico cuyo símbolo es Te y su número atómico es 52. Es un metaloide que se encuentra en el grupo 16 y el periodo 5 de la Tabla periódica de los elementos.
Fue descubierto en 1782 en minerales de oro por Franz-Joseph Müller von Reichenstein, inspector jefe de minas en Transilvania (Rumanía), denominándolo metallum problematicum. En principio se confundió el telurio con el antimonio. Fue Martin Heinrich Klaproth, en 1798, quien examinó el «metal problemático» de Müller y lo llamó telurio.
El telurio es un elemento relativamente estable, insoluble en agua y ácido clorhídrico, pero soluble en ácido nítrico y en agua regia. Reacciona con un exceso de cloro para formar dicloruro de teluro, TeCl2 y tetracloruro de teluro, TeCl4. Se oxida con ácido nítrico y produce dióxido de teluro, TeO2, y con ácido crómico para dar ácido telúrico, H2TeO4. En combinación con el hidrógeno y ciertos metales, forma telururos, como el telururo de hidrógeno, H2Te, y el telururo de sodio, Na2Te. El teluro tiene un punto de fusión de 452° C, un punto de ebullición de 990° C, y una densidad relativa de 6,25. Su masa atómica es 127,60.
Los compuestos de telurio se usan ampliamente en la química orgánica sintética para la reducción y oxidación, ciclofuncionalización, deshalogenación, reacciones de generación de carbaniones y eliminación de grupos protectores.Los compuestos organometálicos son intermedios en la síntesis de aminas, dioles y productos naturales.El telurio es un componente de importancia clave en los catalizadores de óxidos mixtos de alto rendimiento para la oxidación selectiva catalítica heterogénea de propano a ácido acrílico.En presencia de vapor de agua, la superficie del catalizador se enriquece en telurio y vanadio lo que se traduce en la mejora de la producción de ácido acrílico.El telurio puede usarse en sensores de amoníaco y cristales de telurita.
Abundancia y obtención
El telurio puede obtenerse combinado con oro en la calaverita, un mineral metálico relativamente poco abundante.
En abril de 2017 se publicó el hallazgo del mayor yacimiento de telurio del mundo, en aguas de las Islas Canarias (España), en los montes submarinos situados dentro de las aguas canarias llamadas "las abuelas de Canarias" (Drago, Bimbache, Ico, Pelicar, Malpaso, Tortuga e Infinito y Las Abuelas). Se calcula que el yacimiento tiene un total de unas 2670 toneladas de Telurio, unas 50 000 veces más que el hallazgo más grande encontrado hasta ahora.
POLONIO
El polonio es un elemento químico en la tabla periódica de los elementos cuyo símbolo es Po y su número atómico es 84. Se trata de un raro metal altamente radiactivo, químicamente similar al telurio y al bismuto, presente en minerales de uranio.
Características
Esta sustancia se disuelve con mucha facilidad en ácidos, pero es sólo ligeramente soluble en alcalinos. Está químicamente relacionado con el teluro y el bismuto. El polonio es un metal volátil, reducible al 50% tras 45 horas al aire a una temperatura de 54,8 °C (328 K). Ninguno de los 50 isotopos [numero estimado] de polonio es estable. Es extremadamente tóxico y altamente radiactivo. Se ha encontrado polonio en minerales de uranio, humo de tabaco y como contaminante. Todos los elementos a partir del polonio son significativamente radiactivos. Se encuentra en el grupo 16 y su número atómico es 84.
Aplicaciones
Mezclado o aleado con berilio, el polonio puede ser una fuente de neutrones.
Se utiliza también en dispositivos destinados a la eliminación de carga estática, en cepillos especiales para eliminar el polvo acumulado en películas fotográficas y también en fuentes de calor para satélites artificiales o sondas espaciales.
UNUNHEXIO

El livermorio (anteriormente llamado ununhexio, Uuh o nectariel, nectartén o nectartenio con símbolo Nc)es el nombre del elemento sintético de la tabla periódica cuyo símbolo es Lv y su número atómico es 116.
FLÚOR

El flúor es el elemento químico de número atómico 9 situado en el grupo de los halógenos (grupo 17) de la tabla periódica de los elementos. Su símbolo es F.
Es un gas a temperatura ambiente, de color amarillo pálido, formado por moléculas diatómicas F2. Es el más electronegativo y reactivo de todos los elementos. En forma pura es altamente peligroso, causando graves quemaduras químicas al contacto con la piel.
Características principales
En disolución acuosa, el flúor se presenta normalmente en forma de ion fluoruro, F-. Otras formas son fluorocomplejos como el [FeF4]-, o el H2F+.
Los fluoruros son compuestos en los que el ion fluoruro se combina con algún resto cargado positivamente.
Aplicaciones
- El politetrafluoroetileno (PTFE), también denominado teflón, se obtiene a través de la polimerización de tetrafluoroetileno que a su vez es generado a partir de clorodifluorometano, que se obtiene finalmente a partir de la fluoración del correspondiente derivado halogenado con fluoruro de hidrógeno (HF).
- También a partir de HF se obtienen clorofluorocarburos (CFC), hidroclorofluorocarburos (HClFC) e hidrofluorocarburos (HFC).
- Se emplea flúor en la síntesis del hexafluoruro de uranio, UF6, es el gas más pesado conocido y se emplea en el enriquecimiento de uranio 235U.
- El fluoruro de hidrógeno se emplea en la obtención de criolita sintética, Na3AlF6, la cual se usa en el proceso de obtención de aluminio.
- Hay distintas sales de flúor con variadas aplicaciones[cita requerida]. El fluoruro de sodio, NaF, se emplea como agente fluorante; el difluoruro de amonio, NH4HF2, se emplea en el tratamiento de superficies, anodizado del aluminio, o en la industria del vidrio; el trifluoruro de boro, BF3, se emplea como catalizador; etc.
- Algunos fluoruros se añaden a las pastas de dientes para la prevención de caries (principalmente el fluoruro de sodio).
- En algunos países se añade fluoruro a las aguas potables para prevenir la aparición de caries, de lo que se suele avisar a la población. Algunos países como Estados Unidos o Australia fluoran el agua potable, mientras que otros como Alemania lo prohíben.[cita requerida]
- Se emplea flúor monoatómico en la fabricación de semiconductores.
- El hexafluoruro de azufre, SF6, es un gas dieléctrico con aplicaciones electrónicas. Este gas contribuye al efecto invernadero y está recogido en el Protocolo de Kioto.
Abundancia y obtención
LE FALTARON GRUPOS POR CONSULTAR 4,0
ResponderEliminarDEFINITIVA 4,5